Rťaction de substitution nuclťophile SN2
on s'intťresse ŗ la rťaction entre :
| un dťrivť monohalogťnť (molťcule d'alcane RH possťdant en substitution d'un atome d'hydrogťne un halogŤne X comme le chlore, le brome ou l'iode) | |
| et un nuclťophile (groupement d'atome Y ayant une forte rťactivitť pour les rťgions possťdant un dťfaut d'ťlectrons, comme l'eau, l'ammoniac, les alcolates...). |
les mťcanismes rťactionnels laissent ŗ penser que deux interprťtations sont
possibles, l'une d'elle fait appel ŗ une seul rťaction ťlťmentaire: ![]()
La loi de vitesse associťe va donc se mettre sous la forme v=k[RX][Y]. On a donc un ordre 2 pour la vitesse.
Dťgťnťrescence de l'ordre
Nous allons appliquer ce modŤle ŗ la rťaction suivante: On verse un tout petit peu d'eau (c mol/l) dans une solution de chloroťthane RCl (C mole/l , C>>c ) et on surveille l'apparition d'ťthanol ROH. La cause est ici l'apport d'eau et l'effet l'apparition d'ťthanol.
en notant x l'avancement volumique de la rťaction, on a [ROH]=x. au maximum x sera ťgal ŗ c, on peut donc faire l'approximation suivante [RCl]=C . Cela revient ŗ considťrer que l'ordre de la rťcation n'est plus que 1!
Calcul de la solution
on obtient:: 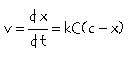 .
.
il n'y a plus qu'a poser ![]()
On reconnait l'ťquation diffťrentielle du premier
ordre avec sa solution exponentielle: ![]()